Neurosarcoïdose
Date de dernière édition : 22/09/2024
La neurosarcoïdose regroupe l'ensemble des atteintes neurologiques de la sarcoïdose, pathologie inflammatoire multi-systémique granulomateuse d'étiologie inconnue.
Il existe une relative imprécision sémantique, le terme de "neurosarcoïdose" étant fréquemment utilisé en pratique pour désigner toute manifestation clinique neurologique d'une sarcoïdose... Ainsi, une paralysie faciale résultant de la compression du nerf VII secondaire à une infiltration parotidienne sarcoïdosique relève-t-elle d'une neurosarcoïdose ? Ces nuances ne sont pas dénuées d'importance puisqu'elles ont des implications en termes de projet thérapeutique et de suivi.
Une neurosarcoïdose se rencontre dans 5 à 15% des cas de sarcoïdoses. Dans environs 50% des neurosarcoïdoses, la symptomatologie neurologique est inaugurale et dans environs 10% la maladie demeurera limitée au système nerveux. L'évocation diagnostique est facile en cas de survenue d'atteintes neurologiques inexpliquées dans le cadre d'une sarcoïdose connue ou de la coexistence avec des signes systémiques mais très difficile en cas de symptômes neurologiques isolés inauguraux.
Les manifestations extra-neurologiques et généralités de la sarcoïdose sont abordées dans le cadre d'un chapitre particulier :
Eléments de physiopathologie
La physiopathogénie de la sarcoïdose, toujours hypothétique, est présumée impliquer des facteurs environnementaux sur un terrain multigénique prédisposant. Bien que de nombreux agents environnementaux (pollens, pesticides, insecticides, antigènes de mycobactéries, traitement par interferon alpha,...) et gènes aient été évoqués sur base de cas, aucun n'a été jusqu'ici été démontré susceptible d'induire la maladie.
Certains génotypes des complexes HLA-DQ et HLA-DR ont cependant été liés à la sacoïdose sans qu'il soit possible de déterminer s'ils favorisaient la survenue de la maladie ou en modulaient l'expression phénotypique. Il existe par ailleurs une notion d'hérédité et les malades ont 5,8 fois plus de chance que les sujets sains de compter un cas index dans la famille.
Quoi qu'il en soit, on observe une accumulation et une activation locale de lymphocyte T helpers CD4+ déclenchant une cascade inflammatoire aboutissant à la formation de granulomes non caséeux. Ces granulomes peuvent se former dans tous les organes mais touchent préférentiellement les poumons. Une des complications redoutées de ce phénomène est l'évolution vers une fibrose pulmonaire dont la genèse reste obscure.
L'atteinte neurologique quant-à-elle peut être directe, par une infiltration granulomateuse méningée, ou indirecte, par compression par un granulome de voisinage (ex : paralysie faciale sur compression du nerf par une parotidite). Une infiltration méningée peut rester localisée, diffuser aux racines des nerfs crâniens et rachidiens et/ ou envahir les vaisseaux radiculaires, médullaires ou cérébraux (vasculite granulomateuse) et, par ce biais, léser le parenchyme.
Atteintes neurologiques
Atteintes des "nerfs crâniens" (25-70%)
Ces atteintes se rencontrent dans 25 à 70% des neurosarcoïdoses. Elles sont généralement multiples, récidivantes, alternantes et d'évolution spontanément favorable ou sous corticothérapie. Dans 30 à 50% des cas, elles s'associent à une atteinte centrale ou d'autres atteintes périphériques.
Toutes les paires crâniennes peuvent être touchés : VII (≈ 30%) > II (≈ 20%) > VIII (≈ 15%) > nerfs oculomoteurs (≈ 10%) > V (≈ 10%) > autres (rare). Les manifestations les plus fréquentes sont cependant :
- Nerf facial (VII) :
- Se manifeste par une paralysie faciale
- Son atteinte est associée à l'atteinte d'un autre nerf crânien dans ≈ 66% des cas.
- Les rechutes et atteintes bilatérales ou à bascule sont fréquentes.
- Le classique syndrome de Heerfordt (atteinte du VII + parotidite + iridocyclite), pathognomonique, n'est retrouvé que dans 5% des cas.
- Mécanismes physiopathologiques possibles : parotidite, compression au foramen stylomastoïdien, infiltration à partir des méninges, atteinte intra-axiale.
- Nerf optique (II) :
- Son atteinte réalise généralement une névrite optique sub-aiguë, uni ou bilatérale, se manifestant par une diminution de l'acuité visuelle et/ ou une dyschromatopsie et/ ou des douleurs aux mouvements oculaires.
- Peut passer inaperçue du fait d'une lente évolution ou d'une uvéite concomitante (très fréquente).
- Très bonne récupération sous corticoïdes dans ≈ 50% des cas mais fréqquemment cortico-dépendante.
- Nerf auditif (VIII)
- Clinique consistant généralement en une surdité progressive ou fluctuante, uni ou bilatérale, fréquemment accompagnée de manifestations vestibulaires.
- Nerfs oculomoteurs (III, IV, VI) et nerf trijumeau (V) : atteintes (troubles oculomoteurs et troubles sensitifs faciaux) rarement révélatrices et peu évocatrices, sauf en cas d'association à d'autres atteintes neurologiques ou de manifestations systémiques.
Atteintes et manifestations encéphaliques (36-66%)
Des manifestations encéphaliques se rencontrent dans 36 à 66% des cas de neurosarcoïdoses. Elles sont très variées et peu évocatrices, les plus fréquentes étant :
- Encéphalopathies (altération globale des fonctions supérieures) et troubles neuro-psychiques :
- Le plus souvent sur sur hydrocéphalie, atteinte hypothalamo-hypophysaire ou frontale.
- A noter que les mêmes manifestations cliniques peuvent également être secondaires aux troubles métaboliques d'une sarcoïdose sans atteinte neurologique directe et ne rentrant donc pas dans le cadre d'une neurosarcoïdose. Ex : troubles neuro-psychiatriques sur hypercalcémie dans le cadre d'une sarcoïdose rénale.
- Hydrocéphalie :
- Fréquemment décrite mais généralement asymptomatique.
- Lorsqu'elle est symptomatique : céphalées, bradypsychie, instabilité à la marche.
- Résulte généralement d'une obstruction par défaut de résorption sur arachnoïdite granulomateuse.
- Atteintes hypothalamo-hypophysaires :
- Manifestations : diabète insipide, hyperprolactinémie, syndrome de sécrétion inappropriée en hormone anti-diurétique, aménorrhée, troubles du sommeil et du comportement, hyperthermie,…
- Résulte généralement d'une infiltration sous-épendymaire du troisième ventricule.
- Lésions pseudo-tumorales (uniques ou multiples) : rarement symptomatiques, réalisant exceptionnellement un tableau d'hypertension intracrânienne.
- Crises épileptiques
- Atteintes cérébelleuses ou du tronc cérébral
- Exceptionnels : accidents vasculaires cérébraux ischémiques (sur vasculite ou cardiopathie emboligène), thrombose veineuse cérébrale, hémorragie sous-arachnoïdienne, mouvements anormaux et syndromes parkinsoniens.
Neuropathies périphériques hors paires crâniennes (≈ 20%)
Toutes les formes sont possibles : mononeuropathies, multineuropathies (++ cubital et sciatique poplité externe), polyneuropathies (++ axonales sub-aiguës à chroniques), polyradiculonévrites aiguës de type Guillain-Barré. On note également une incidence accrue des syndromes de canaux carpiens. Une atteinte associée des nerfs crâniens doit faire évoquer le diagnostic.
Méningites sarcoïdiennes (≈ 20%)
Les méningites sarcoïdiennes réalisent un tableau de syndrome méningé (sub)-aigu à chronique. A différencier des "méningites" asymptomatiques (anomalies du liquide céphalo-rachidien [LCR] sans manifestation clinique) présentes dans 50-80% des neurosarcoïdoses.
Elle sont généralement corticosensibles mais souvent récurrentes et corticodépendantes.
Atteintes médullaires (≈ 10%)
Elles se rencontrent dans ≈ 10% des neurosarcoïdoses, sont généralement associées à une méningo-encéphalite, de localisation le plus souvent cervicale et se manifestant le plus souvent par une tétra ou paraparésie progressive (on rencontre plus rarement une myélopathie transverse ou un syndrome de la queue de cheval). Le pronostic de récupération est réputé médiocre bien que dépendant du type de lésion sous-jacente.
Elles peuvent résulter de granulomes intramédullaires ou périduraux, d'une arachnoïdite ou d'infarctus médullaires (vasculite granulomateuse, cardio-emboliques,...).
Myopathies
Elles sont citées à titre d'information. Leur place dans ce cadre nosologique est discutable. Par ailleurs, des atteintes musculaires sont fréquemment retrouvées à l'anatomo-pathologie dans les neurosarcoïdoses, mais de véritables myopathies cliniques sont exceptionnelles.
Dans ce cas, il s'agit généralement d'une myopathie proximale d'évolution chronique et symétrique avec amyotrophie et crampes. Le dosage des CK est généralement normal. Plus rarement, il s'agit d'une forme pseudo-myositique, avec présence plus fréquente d'un syndrome inflammatoire, de myalgies et de CK élevées.
Les formes les plus sévères peuvent engager le pronostic vital.
Particularités diagnostiques et diagnostic différentiel
Le diagnostic de neurosarcoïdose est souvent difficile, particulièrement en l'absence de sarcoïdose connue, et le diagnostic différentiel large selon la présentation clinico-radiologique (à titre d'exemple : connectivites, vasculites, maladie de Whipple, méningites carcinomateuse ou tuberculeuse ou à germes atypiques, syndrome paranéoplasique, borréliose, HIV, sclérose en plaques, tumeurs, neurosyphilis, autres causes d'hydrocéphalie chronique,…).
Quoi qu'il en soit, une neurosarcoïdose est à évoquer systématiquement en cas de :
- Troubles neurologiques dans un contexte de sarcoïdose connue
- Troubles neurologiques associés à un syndrome systémique, une parotidite, un érythème noueux ou un syndrome fébrile inexpliqué
- Atteinte concomitante des systèmes nerveux périphérique et central
- Atteintes multiples, récidivantes, bilatérales ou à bascule de paires crâniennes
Examens complémentaires
En cas de suspicion clinique raisonnable → bilan systémique classique d'une sarcoïdose à compléter par :
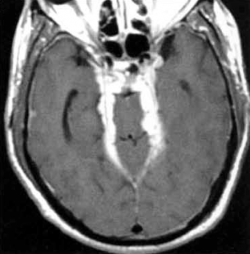
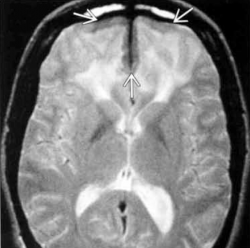
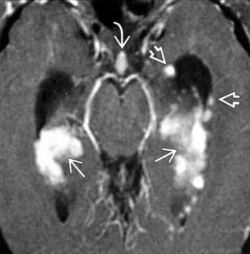
- Imagerie cérébrale et/ ou médullaire : sensibilité variable selon le type de lésion, peu spécifique, très grande variété de lésions.
- CT-scanner : possibles lésions hyperdenses, infiltration méningée prenant le contraste, hydrocéphalie, lésions ostéolytiques,…
- IRM avec gadolinium et diffusion : hydrocéphalie, infarctus lacunaires, lésions méningées diffuses ou nodulaires (isodenses en T1, hypodenses en T2, prenant le gadolinium), lésions parenchymateuses uniques ou multiples prenant ou non le gadolinium, vasculites, plages d'œdème vasogénique, lésion des plexus choroïdes,…
- Ponction lombaire (PL) : anormale dans 50 à 80% des cas. Anomalies aspécifiques (pléiocytose le plus souvent lymphocytaire, hyperprotéinorachie, IgG et/ ou albumine augmentées, hypoglycorachie,…). Le dosage de l'ACE ne présente pas d'intérêt.
- Biopsie méningée ou parenchymateuse : de manière générale, le diagnostic de sarcoïdose suppose l'obtention d'une preuve anatomo-pathologique. Au vu du caractère particulièrement invasif des biopsies méningées ou parenchymateuses, elle ne devraient être effectuées qu'en l'absence d'autre tissu biopsiable et en fonction du contexte clinique. Les biopsies de nerfs périphériques sont quant à elles de rentabilité très médiocre.
- Vitesses de conduction nerveuses (VCN) et électromyographie (EMG) : utiles pour objectiver la présence d'une neuropathie périphérique et son évolution mais non spécifique pour le diagnostic de neurosarcoïdose
Prise en charge thérapeutiques et suivi - Particularités
La neurosarcoïdose rentre dans le cadre d'une pathologie systémique → tenir compte des autres atteintes éventuelles pour l'élaboration d'un plan de traitement et de suivi.
De manière générale, les modalités de traitement de la sarcoïdose reposent sur une evidence faible et quasi inexistante concernant la neurosarcoïdose. Il existe cependant un consensus dans ce dernier cas quant à l'utilisation en première intention de corticoïdes ou d'immunosuppresseurs. Les modalités du traitement (corticoïdes ou immunosuppresseurs, per os ou IV, avec ou sans relais au long cours) restent à déterminer au cas par cas selon la sévérité clinique, l'extension des lésions et les atteintes systémiques associées, la topographie des lésions et le mécanisme lésionnel (une neuropathie sur compression par un granulome parotidien n'ayant pas la même signification qu'une infiltration directe du nerf). Idéalement, le plan thérapeutique et de suivi devraît être élaboré en concertation entre un interniste, un neurologue et les spécialistes des autres organes atteints le cas échéant.
Exemple de schéma thérapeutique :
- Traitement de première intention = corticothérapie :
- Formes mineures : paralysie faciale périphérique ou méningite aseptique cliniquement patente
- methylprednisolone 0,5 à 1 mg/ kg/ jour durant 15 jours puis schéma dégressif sur 1 à 6 mois selon évolution clinique
- Formes modérées : myopathies diffuses, autres neuropathies, masses méningées ou parenchymateuses,... + formes mineures en échec thérapeutique ou récidivantes
- methylprednisolone 0,5 à 1 mg/ kg/ jour durant 30 jours puis schéma dégressif sur 1 à 12 mois selon évolution clinique
- en cas de réponse thérapeutique positive mais insuffisante ou de cortico-dépendance :
- ajouter un cytotoxique : methotrexate ou azathioprine
- Formes sévères : patients dont les manifestations cliniques sont particulièrement sévères ou handicapantes + formes modérées en échec thérapeutique ou récidivantes
- cure IV methylprednisolone 20 mg/ kg/ jour durant 3 jours → relais PO 0,5 à 1 mg/ kg/ jour durant 30 jours puis schéma dégressif sur 1 à 12 mois
- chez des patients sélectionnés ou en cas d'échec thérapeutique :
- ajouter du cyclophosphamide
- Formes mineures : paralysie faciale périphérique ou méningite aseptique cliniquement patente
- Traitements de deuxième intention (en cas de contre-indication aux corticoïdes ou de cortico-résistance) : maintien d'une corticothérapie d'entretien si possible (ex : 8 mg/ jour) + immunosuppresseur :
- Mycophenolate mofetil, azathioprine, cyclophosphamide, chlorambucil, cladribine
- Infliximab pour les cas sévères : cures IV de 5 mg/ kg du poids idéal à répéter selon décours clinique
- Divers : hydroxychloroquine, pentoxifylline
- Indication des autres traitements :
- Hydrocéphalie aiguë : dérivation ventriculo-péritonéale (suivi particulier : risques de dysfonctionnements ++ vu l'inflammation)
- Masse menaçante réfractaire au traitement médical : exérèse chirurgicale, exceptionnellement nécessaire
- Maladie très agressive et échec des corticoïdes et de minimum 2 immunosuppresseurs : envisager radiothérapie (risque d'encéphalopathie radique tardive en cas d'irradiation panencéphalique !)
Suivi clinico-radiologique minimum 1x/ 3 mois tant que le patient est traité par corticoïdes ou immunosuppresseurs. L'utilité d'un suivi électrophysiologique des atteintes du système périphérique est discutée. La répétition de ponctions lombaires n'est pas utile voire nuisible (fréquente persistance d'anomalies du liquide céphalo-rachidien sans signification clinique).
Bibliographie
Bagnato F et al., Neurosarcoidosis: diagnosis, therapy and biomarkers, Expert Rev Neurother, 2015 May, 15(5):533-48
Bradley WG et al., Neurology in clinical practice, 5th ed., Butterworth-Heinemann, e-dition, 2007
Cremers JP et al., Multinational evidence-based World Association of Sarcoidosis and Other Granulomatous Disorders recommendations for the use of methotrexate in sarcoidosis: integrating systematic literature research and expert opinion of sarcoidologists worldwide, Curr Opin Pulm Med, 2013, 19(5): p. 545-61
Dubas F et al., Neurosarcoïdose, Encycl Méd Chir, Neurologie, 17-168-A-10, 2001
Foundation for sarcoidosis research, Sarcoidosis treatment guidelines, 2015
Iannuzzi MC et al., Sarcoidosis, N Engl J Med, 2007, 357:2153-65
Osborn AG, Diagnostic imaging : brain, Amirsys, USA, 2d ed., 2009
Stern BJ et al., Neurologic sarcoidosis, uptodate, 2015
Thomas KW et al., Sarcoidosis, JAMA, 2003; 289:3300-3