« Gestion des surconsommation et surprescription des antibiotiques » : différence entre les versions
(Page créée avec « La surconsommation en antibiotiques représente un problème de santé publique majeur car cette surconsommation est le facteur principal à l’origine de la résistance des... ») |
m (Remplacement de texte : « Shanan Khairi, MD » par « Dr Shanan Khairi, MD ») |
||
| (14 versions intermédiaires par le même utilisateur non affichées) | |||
| Ligne 1 : | Ligne 1 : | ||
La surconsommation | <p style="text-align: left;">La '''surconsommation des antibiotiques''', principal facteur à l’origine de la [[Antibiorésistance_(résistance_aux_antibiotiques)|résistance aux antibiotiques]], représente un problème de santé publique majeur. Ceci est vrai à l'échelle mondiale, cette problématique étant à l'avant-plan des préoccupations de l'Organisation Mondiale de la Santé (OMS), mais bien plus encore pour certains pays développés apparaissant particulièrement irresponsables en la matière, aux premiers rangs desquels la Belgique et la France.</p> | ||
== Le cas particulier de la Belgique et de la France == | |||
Le programme de surveillance européen pointe que la | <p style="text-align: left;">Le programme de surveillance européen pointe tant la Belgique que la France comme de grandes surconsommatrices d’antibiotiques, tant en hospitalisation qu’en pratique ambulatoire. Il en découle des taux d'antibiorésistance plus élevés que ceux par exemple observés aux Pays-Bas, pays nettement moins consommateur (Belgique et France à 30 - 31.5 DDD/ 1000 jours-habitants ; Pays-Bas : 12.3 DDD/ 1000 jours-habitants). Cette surconsommation / suprescription étant principalement observée en pratique ambulatoire.</p><p style="text-align: left;">Ceci a justifié le déploiement en Belgique de stratégies "d’antimicrobial stewardship" et a justifié d’ailleurs les premières mesures de forfaitarisation des médicaments à l’hôpital (financement non pas de ce qui est prescrit, mais d’un montant fixe, fonction de la pathologie des patients de l’hôpital en question) et de campagnes de promotion orientées vers les médecins généralistes et le grand public.</p> | ||
{{Modèle:Thumbc|ConsoAB.png|500px|Consommation d'antibiotiques par voie systémique dans les pays de l'Union Européenne, exprimée en DDD pour 1000 habitants par jour (ECDC, 2012.}} | |||
Ceci a justifié le déploiement de stratégies d’antimicrobial stewardship et a justifié d’ailleurs les premières mesures de forfaitarisation des médicaments à l’hôpital ( | |||
== Quelles solutions ? == | |||
<p style="text-align: left;">L’antimicrobial stewardship consiste à accompagner l’utilisation des antibiotiques à l’échelle d’un prescripteur, un ensemble de prescripteurs, une institution de soins ou un pays, d’un cadre promouvant le bon usage de ceux-ci.</p><p style="text-align: left;">Plusieurs stratégies complémentaires sont ou devraient être en place :</p><p style="text-align: left;">- Limitation du choix des spécialités disponibles dans un hôpital (choix élaboré de manière multidisciplinaire par les infectiologues, hygiénistes, pharmaciens, microbiologistes et utilisateurs),</p><p style="text-align: left;">- Formation / information des prescripteurs (guidelines locaux, …),</p><p style="text-align: left;">- Contrôle a priori ou a posteriori de la sortie de certains antibiotiques et de leur utilisation,</p><p style="text-align: left;">- Évaluation de la qualité de la prescription à l’échelle individuelle (indication, choix, voie d’administration, posologie, durée, toxicité, …) et feed-back sous forme d’un % de traitements adéquats (souvent proche de 50% seulement …),</p><p style="text-align: left;">- Évaluation de la quantité utilisée dans un hôpital, ou en ambulatoire, local, ou national et comparaison par type de pathologies (APR-DRG),</p><p style="text-align: left;">- ….</p><p style="text-align: left;">Le prescripteur doit s’intégrer dans une démarche proactive de qualité dans l’utilisation des antibiotiques. Cette démarche passe par la considération d’indicateurs qualité permettant de mesurer la pertinence de l’utilisation des antibiotiques.</p><p style="text-align: left;">Indicateurs à l’échelle hospitalière :</p> | |||
*Consommation totale | *Consommation totale | ||
*Consommation relative des différentes classes | *Consommation relative des différentes classes | ||
| Ligne 41 : | Ligne 12 : | ||
*Analyse par pathologie (APR-DRG) | *Analyse par pathologie (APR-DRG) | ||
*% compliance guidelines thérapeutiques et prophylactiques | *% compliance guidelines thérapeutiques et prophylactiques | ||
<p style="text-align: left;"> </p><p style="text-align: left;">Il est également indispensable de mettre en place des indicateurs qualité permettant d’évaluer la qualité au niveau de chaque patient. Ceci passe par la définition de guidelines de préférence EBM et ensuite d’une évaluation de chacune des étapes du traitement individuel, à savoir :</p> | |||
| |||
Il est également indispensable de mettre en place des indicateurs qualité permettant d’évaluer la qualité au niveau de chaque patient. Ceci passe par la définition de guidelines de préférence EBM et ensuite d’une évaluation de chacune des étapes du traitement individuel, à savoir : | |||
*Qualité des données reprises dans le dossier médical permettant de justifier le traitement | *Qualité des données reprises dans le dossier médical permettant de justifier le traitement | ||
*Indication de traiter | *Indication de traiter | ||
| Ligne 51 : | Ligne 18 : | ||
*Durée? | *Durée? | ||
*Posologie, voie, timing? | *Posologie, voie, timing? | ||
<p style="text-align: left;"> </p><p style="text-align: left;">Il s’agit là d’une application à la prescription des antibiotiques de la méthodologie « Qualité », étape indispensable qui s’inscrit dans le cadre plus vaste de l’introduction de ces outils pour améliorer la pratique médicale.</p><p style="text-align: left;">En effet, on constate dans tous les domaines un grand écart entre les connaissances théoriques (référentiels EBM) et leur application sur le terrain. Les outils qualité (notamment par exemple la roue de Deming, la mise en place d’indicateurs, etc.) ont pour objectif d’asseoir ces stratégies dans le système complexe des soins de santé dans le but d’apporter un maximum de bénéfice au patient en particulier et à la santé publique en général.</p><p style="text-align: left;">L’enjeu majeur de la pérennité des agents anti-infectieux rend les acteurs médicaux dans ce domaine particulièrement sensibles à ces nouveaux outils et leur apport et doit absolument avoir le soutien et la participation active de tous les médecins.</p><div><p style="text-align: left;"></p> | |||
| |||
Il s’agit là d’une application à la prescription des antibiotiques de la méthodologie « Qualité », étape indispensable qui s’inscrit dans le cadre plus vaste de l’introduction de ces outils pour améliorer la pratique médicale. | |||
En effet, on constate dans tous les domaines un grand écart entre les connaissances théoriques (référentiels EBM) et leur application sur le terrain. Les outils qualité (notamment par exemple la roue de Deming, la mise en place d’indicateurs, etc.) ont pour objectif d’asseoir ces stratégies dans le système complexe des soins de santé dans le but d’apporter un maximum de bénéfice au patient en particulier et à la santé publique en général. | |||
L’enjeu majeur de la pérennité des agents anti-infectieux rend les acteurs médicaux dans ce domaine particulièrement sensibles à ces nouveaux outils et leur apport et doit absolument avoir le soutien et la participation active de tous les médecins. | |||
<div>< | |||
---- | ---- | ||
<div id="ftn1"> | <div id="ftn1"><p style="text-align: left;">[[#_ftnref1|[1]]] La comparaison de la consommation entre 2 sites de prescription (2 hôpitaux ou 2 pays par ex) passe par la conversion du volume utilisé en Defined Daily Doses internationales (ex un total de 120 g de ceftazidime correspond à 30 x la dose internationale standardisée qui est de 4 g/jour = 30 DDD). La consommation peut alors être exprimée en DDD/1000 jours-patients hospitalisés ou DDD/1000 jours-habitants.</p></div></div> | ||
[[#_ftnref1|[1]]] La comparaison de la consommation entre 2 sites de prescription (2 hôpitaux ou 2 pays par ex) passe par la conversion du volume utilisé en Defined Daily Doses internationales (ex un total de 120 g de ceftazidime correspond à 30 x la dose internationale standardisée qui est de 4 g/jour = 30 DDD). La consommation peut alors être exprimée en DDD/1000 jours-patients hospitalisés ou DDD/1000 jours-habitants. | == Auteur(s) == | ||
</div></div> | <p style="text-align: left;">Pr [[Utilisateur:Baudouin Byl|Baudouin Byl]], MD, PhD</p><p style="text-align: left;">(Mis en forme, revu et modifié par Dr [[Utilisateur:Shanan Khairi|Shanan Khairi]], MD) {{Modèle:Catégorie|Infectiologie}}{{Modèle:Catégorie|Pharmacologie clinique}}{{Modèle:Catégorie|Thérapie anti-infectieuse}}{{Modèle:Catégorie|Santé publique}}</p> | ||
Version actuelle datée du 4 novembre 2022 à 08:42
La surconsommation des antibiotiques, principal facteur à l’origine de la résistance aux antibiotiques, représente un problème de santé publique majeur. Ceci est vrai à l'échelle mondiale, cette problématique étant à l'avant-plan des préoccupations de l'Organisation Mondiale de la Santé (OMS), mais bien plus encore pour certains pays développés apparaissant particulièrement irresponsables en la matière, aux premiers rangs desquels la Belgique et la France.
Le cas particulier de la Belgique et de la France
Le programme de surveillance européen pointe tant la Belgique que la France comme de grandes surconsommatrices d’antibiotiques, tant en hospitalisation qu’en pratique ambulatoire. Il en découle des taux d'antibiorésistance plus élevés que ceux par exemple observés aux Pays-Bas, pays nettement moins consommateur (Belgique et France à 30 - 31.5 DDD/ 1000 jours-habitants ; Pays-Bas : 12.3 DDD/ 1000 jours-habitants). Cette surconsommation / suprescription étant principalement observée en pratique ambulatoire.
Ceci a justifié le déploiement en Belgique de stratégies "d’antimicrobial stewardship" et a justifié d’ailleurs les premières mesures de forfaitarisation des médicaments à l’hôpital (financement non pas de ce qui est prescrit, mais d’un montant fixe, fonction de la pathologie des patients de l’hôpital en question) et de campagnes de promotion orientées vers les médecins généralistes et le grand public.
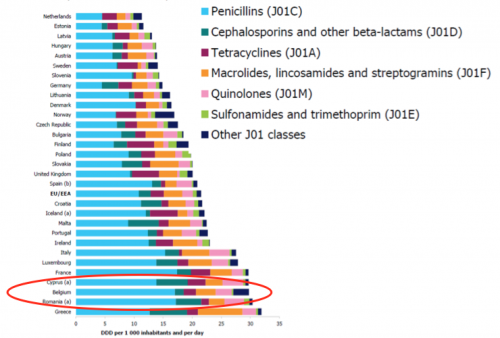 Consommation d'antibiotiques par voie systémique dans les pays de l'Union Européenne, exprimée en DDD pour 1000 habitants par jour (ECDC, 2012. |
Quelles solutions ?
L’antimicrobial stewardship consiste à accompagner l’utilisation des antibiotiques à l’échelle d’un prescripteur, un ensemble de prescripteurs, une institution de soins ou un pays, d’un cadre promouvant le bon usage de ceux-ci.
Plusieurs stratégies complémentaires sont ou devraient être en place :
- Limitation du choix des spécialités disponibles dans un hôpital (choix élaboré de manière multidisciplinaire par les infectiologues, hygiénistes, pharmaciens, microbiologistes et utilisateurs),
- Formation / information des prescripteurs (guidelines locaux, …),
- Contrôle a priori ou a posteriori de la sortie de certains antibiotiques et de leur utilisation,
- Évaluation de la qualité de la prescription à l’échelle individuelle (indication, choix, voie d’administration, posologie, durée, toxicité, …) et feed-back sous forme d’un % de traitements adéquats (souvent proche de 50% seulement …),
- Évaluation de la quantité utilisée dans un hôpital, ou en ambulatoire, local, ou national et comparaison par type de pathologies (APR-DRG),
- ….
Le prescripteur doit s’intégrer dans une démarche proactive de qualité dans l’utilisation des antibiotiques. Cette démarche passe par la considération d’indicateurs qualité permettant de mesurer la pertinence de l’utilisation des antibiotiques.
Indicateurs à l’échelle hospitalière :
- Consommation totale
- Consommation relative des différentes classes
- Ratio spectres étroits / spectres larges
- Proportion IV/per os (ratio)
- Analyse par pathologie (APR-DRG)
- % compliance guidelines thérapeutiques et prophylactiques
Il est également indispensable de mettre en place des indicateurs qualité permettant d’évaluer la qualité au niveau de chaque patient. Ceci passe par la définition de guidelines de préférence EBM et ensuite d’une évaluation de chacune des étapes du traitement individuel, à savoir :
- Qualité des données reprises dans le dossier médical permettant de justifier le traitement
- Indication de traiter
- Choix (le plus efficace? Le moins toxique? Le moins cher? Le spectre le plus étroit?)
- Durée?
- Posologie, voie, timing?
Il s’agit là d’une application à la prescription des antibiotiques de la méthodologie « Qualité », étape indispensable qui s’inscrit dans le cadre plus vaste de l’introduction de ces outils pour améliorer la pratique médicale.
En effet, on constate dans tous les domaines un grand écart entre les connaissances théoriques (référentiels EBM) et leur application sur le terrain. Les outils qualité (notamment par exemple la roue de Deming, la mise en place d’indicateurs, etc.) ont pour objectif d’asseoir ces stratégies dans le système complexe des soins de santé dans le but d’apporter un maximum de bénéfice au patient en particulier et à la santé publique en général.
L’enjeu majeur de la pérennité des agents anti-infectieux rend les acteurs médicaux dans ce domaine particulièrement sensibles à ces nouveaux outils et leur apport et doit absolument avoir le soutien et la participation active de tous les médecins.
[1] La comparaison de la consommation entre 2 sites de prescription (2 hôpitaux ou 2 pays par ex) passe par la conversion du volume utilisé en Defined Daily Doses internationales (ex un total de 120 g de ceftazidime correspond à 30 x la dose internationale standardisée qui est de 4 g/jour = 30 DDD). La consommation peut alors être exprimée en DDD/1000 jours-patients hospitalisés ou DDD/1000 jours-habitants.
Auteur(s)
Pr Baudouin Byl, MD, PhD
(Mis en forme, revu et modifié par Dr Shanan Khairi, MD)

